

重组蛋白是通过基因工程技术人工改造的蛋白质,是现代生物医药研究与生物技术开发的核心支撑技术之一。作为科研试剂的重要组成部分,重组蛋白在信号通路解析、蛋白互作研究、抗体开发、药物筛选及细胞功能实验等众多领域发挥着不可替代的作用。重组蛋白的表达流程,涵盖目的基因获取、表达载体构建、表达系统选择、蛋白表达与纯化等关键环节。
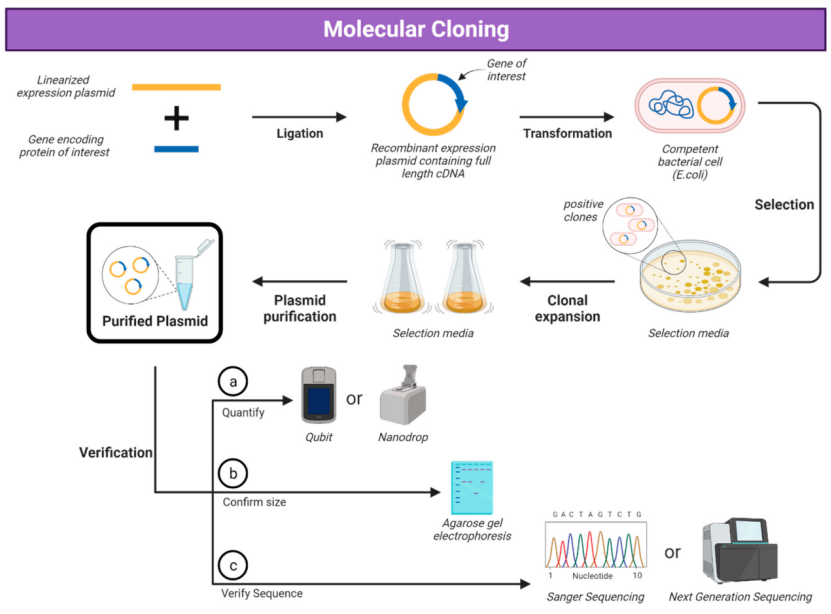
▌基因获取与表达载体构建
根据蛋白序列,通过全基因合成或PCR扩增获得目的DNA片段,将该片段克隆至表达载体中。表达载体需包含强效启动子(如T7、CMV)、筛选标记(如抗生素抗性基因)、复制起点以及用于纯化和检测的标签序列(如His标签、GST标签、Flag标签等)。载体构建完成后,通过测序验证序列正确性,确保无突变、读码框准确,以保证最终蛋白产物结构和功能正确。
▌表达系统的选择与转化
选择合适的表达系统是重组蛋白成功表达的关键。目前常用系统包括原核表达系统(以大肠杆菌为代表)和真核表达系统(如哺乳动物细胞、昆虫细胞、酵母系统)。大肠杆菌表达系统以其操作简便、成本低廉、表达周期短成为最常用的选择,尤其适用于分子量较小、无需复杂翻译后修饰的蛋白。哺乳动物细胞(如HEK293、CHO细胞)能完成最接近天然的人源蛋白翻译后修饰,是生产功能性复杂蛋白的首选。昆虫细胞-杆状病毒系统则在表达膜蛋白或大型蛋白复合物方面具有独特优势。表达系统的选择需综合考量目标蛋白特性、应用需求以及成本效率。
选择合适的表达系统后,将构建好的表达载体导入宿主细胞的过程称为转化(细菌)或转染(真核细胞)。
▌细胞培养与蛋白表达
将转化后的细菌或细胞在优化的培养条件下进行诱导表达。对于大肠杆菌,常用IPTG诱导T7启动子控制下的蛋白表达。诱导时机(菌液密度)、诱导温度、时长及诱导剂浓度均需精细优化,以平衡蛋白表达量与可溶性。
对于哺乳动物或昆虫细胞,转染后需在成分明确、条件稳定的培养体系(如使用无血清培养基)中进行培养。过程需严格控制温度、pH、溶氧及CO₂水平,以维持细胞高活力和高蛋白产率。大规模表达常借助生物反应器,以实现工艺的稳定性和可放大性。
▌细胞收集与裂解
表达结束后,通过离心或过滤收获的细菌或细胞需在适宜缓冲液中进行重悬和裂解,以释放胞内表达的蛋白。裂解方法包括物理法(如高压均质、超声破碎)、化学法(如去垢剂)或酶解法(如溶菌酶)。缓冲液中通常含有蛋白酶抑制剂、还原剂(如DTT)等成分,以保护目标蛋白免受降解或氧化。对于分泌表达的蛋白,则直接从上清液中收集目标产物。
裂解液或上清液经过澄清过滤后,进入核心纯化步骤。基于表达载体所带的亲和标签,最常用的是亲和层析。例如,带有His标签的蛋白可使用固定化金属离子亲和层析(IMAC)进行高效捕获。其他标签如GST、MBP等也有对应的亲和树脂。此步骤能快速从复杂混合物中初步分离目标蛋白。
为进一步提高纯度,常需进行精纯,方法包括离子交换层析(IEX)、疏水相互作用层析(HIC)、分子筛层析(SEC)等。SEC尤其适用于去除聚集体、获得单分散性良好的蛋白样品。对于包涵体形式表达的蛋白,在纯化后还需进行变性与复性操作,通过逐步去除变性剂使蛋白恢复正确天然构象。
重组蛋白作为基础科研与药物研发的关键工具,其表达过程是一套严谨、标准化且高度专业化的技术体系。从基因序列到蛋白质,每一个环节的精准控制都是保障蛋白活性、可重复性及实验结果可靠性的基石。