

在结构生物学研究中,膜蛋白被普遍认为是最具挑战性的研究对象之一。该类蛋白包括 G蛋白偶联受体、离子通道及多种跨膜转运体,其共同特征在于必须同时适应疏水的脂质双分子层内部与亲水的水相环境。从生物物理学角度看,膜蛋白研究的核心难点并非功能复杂性,而是其天然构象对膜环境的高度依赖性。一旦脱离脂质双分子层,膜蛋白跨膜区的疏水表面将暴露于水相,导致显著的自由能惩罚并迅速发生聚集或变性。
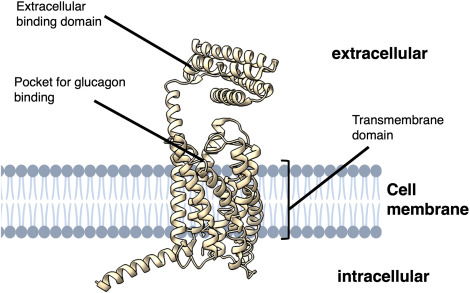
膜蛋白的结构基础在于跨膜结构域(Transmembrane Domain, TMD)。在多数受体和通道蛋白中,TMD 通常由多条 α 螺旋或 β-桶结构组成,其表面富含疏水性氨基酸残基,通过范德华相互作用嵌入脂质双分子层的疏水核心。相对而言,胞外环与胞内环区域则富含极性或带电残基,暴露于水相环境中。
这种高度分区化的拓扑结构使膜蛋白在天然膜中处于最低自由能状态,但也决定了其在离体条件下极易失稳。因此,膜蛋白研究的首要问题并非“提取”,而是在去除天然膜脂的同时,为跨膜区提供一个在物理化学性质上等价的替代环境。
去污剂是膜蛋白研究中最基础的溶解工具。作为典型的两亲性分子,去污剂在浓度超过临界胶束浓度(CMC)后,会自组装形成胶束结构。在膜蛋白溶解过程中,去污剂分子首先插入脂质双分子层,逐步破坏脂质–脂质及脂质–蛋白之间的相互作用,最终形成由去污剂包裹跨膜疏水区的蛋白–去污剂复合物。不同去污剂在疏水强度、胶束尺寸及 CMC 值上的差异,直接影响膜蛋白构象的稳定性。强去污剂能够高效破坏膜结构,但往往破坏蛋白内部疏水核心;相对温和的去污剂则更有利于维持蛋白三级结构,甚至保留部分紧密结合的脂质分子。
尽管去污剂胶束能够实现膜蛋白溶解,但其本质仍是一种高度简化的膜替代体系,无法提供脂质双分子层特有的侧向压力与曲率约束。为更真实地模拟原生膜环境,纳米盘技术被引入膜蛋白研究。纳米盘利用膜支架蛋白将磷脂双分子层限制成尺寸可控的盘状结构,使膜蛋白以接近天然的方式嵌入脂质环境中。相比去污剂体系,纳米盘允许精确控制脂质组成,从而研究特定脂质对膜蛋白构象稳定性的影响。
近年来,苯乙烯–马来酸共聚物(SMA)技术进一步推动了无去污剂溶解策略的发展。SMA 可直接从细胞膜中切割下包含膜蛋白及其周围天然脂质的纳米颗粒,最大程度保留蛋白的脂质微环境,为研究蛋白–脂质相互作用提供了更接近生理状态的模型。
在膜蛋白 X 射线晶体学研究中,脂质立方相(Lipidic Cubic Phase, LCP)技术发挥了关键作用。LCP 是一种具有三维连续曲面的液晶相,在特定脂质与水比例下形成规则的周期性结构。膜蛋白可嵌入弯曲的脂质双分子层,并在其中进行横向扩散。当蛋白浓度达到过饱和状态时,蛋白分子通过亲水区域相互作用或脂质层堆叠形成晶格。这种结晶环境在限制构象波动的同时,维持了接近膜环境的物理约束条件,从而显著提高获得高分辨率结构的成功率。
膜蛋白,尤其是 GPCR,本质上是高度动态的分子,其在不同功能状态之间不断发生构象转换。为获得可解析的稳定结构,常需借助高亲和力配体或构象稳定因子降低其构象熵。配体结合可使蛋白在能量景观中稳定于特定低能态,从而提高结构表征的一致性。
总体而言,膜蛋白结构研究是生物物理学原理的系统应用过程。从去污剂胶束的疏水效应,到纳米盘与脂质立方相对膜环境的重构,每一种技术路径都旨在在离体条件下重建膜蛋白的天然能量状态。对这些物理机制的深入理解,是实现膜蛋白稳定解析与结构表征的理论基础。